भारत बायोटेक के Nasal Booster डोज़ ट्रायल को मिली मंजूरी
नई दिल्ली: Covaxin निर्माता भारत बायोटेक को कोवैक्सिन की दोनों खुराक लेने वाले लोगों पर इंट्रानैसल बूस्टर (Nasal Booster) खुराक के तीसरे चरण के क्लिनिकल परीक्षण करने की मंजूरी मिल गई है।
ड्रग कंट्रोलर जनरल ऑफ इंडिया ने आज तीसरे चरण के परीक्षणों के लिए हरी झंडी दे दी। परीक्षण देश में नौ स्थानों पर आयोजित किए जाएंगे।
बड़े पैमाने पर टीकाकरण अभियान में बूस्टर के रूप में इंट्रानैसल वैक्सीन को प्रशासित करना आसान होगा।
Nasal Booster संक्रमण को रोकने में प्रभावी
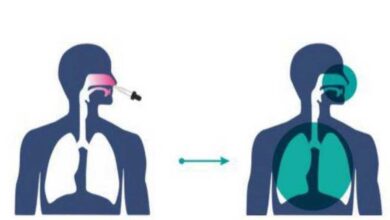
भारत बायोटेक ने कहा है कि Nasal Booster, BBV154, संक्रमण के स्थल पर प्रतिरक्षा प्रतिक्रिया को उत्तेजित करता है, नाक और संक्रमण को रोकने और COVID-19 के संचरण में बहुत प्रभावी है।
इसने यह भी रेखांकित किया है कि Nasal Booster डोज़ को कितनी आसानी से प्रशासित किया जा सकता है और यह तथ्य कि इसके लिए प्रशिक्षित स्वास्थ्य कर्मियों की आवश्यकता नहीं होगी।
हैदराबाद स्थित वैक्सीन निर्माता ने पिछले महीने नाक के टीके के तीसरे चरण के परीक्षण के लिए दवा नियामक की मंजूरी मांगी थी।
भारत बायोटेक के कोवैक्सिन और सीरम इंस्टीट्यूट ऑफ इंडिया के कोविशील्ड को बाजार में बिक्री के लिए मंजूरी मिलने के तुरंत बाद नई मंजूरी मिली। हालांकि, इसका मतलब यह नहीं है कि दोनों टीके जल्द ही दुकानों पर उपलब्ध होंगे। जबकि लोग उन्हें अस्पतालों और क्लीनिकों से खरीद सकेंगे, इस पर विवरण की प्रतीक्षा है।
आपातकालीन उपयोग के लिए, सुरक्षा डेटा को भारत के औषधि महानियंत्रक, या DCGI को 15 दिनों के भीतर देना होता है, लेकिन बाजार की मंजूरी के लिए डेटा छह महीने के भीतर नियामक को देना होता है।
दो टीकों की बाजार बिक्री को न्यू ड्रग्स एंड क्लिनिकल ट्रायल रूल्स, 2019 के तहत मंजूरी दी गई थी।
Covaxin निर्माता भारत बायोटेक और कोविशील्ड निर्माता सीरम इंस्टीट्यूट ऑफ इंडिया, या SII ने नियामक को चल रहे नैदानिक परीक्षणों का डेटा दिया था, जिसने 19 जनवरी को COVID-19 पर एक विषय विशेषज्ञ समिति द्वारा अनुमोदन की सिफारिश के बाद बाजार में बिक्री को मंजूरी दी थी।